[오답풀이 정리] semanal 6 (2da - 2)
2022. 10. 9
Quimica: cinética química
1. En la reacción: NH₄¹⁺ (ac ) + NO₂¹⁻ (ac) → N₂ (g) + 2 H₂O (l), se encontró que la ley de velocidad es V = k [NH₄¹⁺][NO₂¹⁻]. En un experimento donde [NO₂¹⁻] = 0,04 M y [NH₄¹⁺] = 0,20 M, la velocidad observada fue 2,15x10⁻⁶ M/s. El valor de k es:
1 point
A) 2,69x10⁻⁴ M⁻¹. s⁻¹
B) 2,69x10⁻⁴ M. s⁻¹
C) 2,69x10⁻¹⁰ M. s⁻¹
D) 2,69x10⁻¹⁰ M⁻¹. s⁻¹
E) 3,69x10⁻¹⁰ M⁻¹. s⁻¹
2. Considere el gráfico de la reacción: A + B → C + D , y responde: (a) ¿cuál es el valor de Ea directa? , (b) ¿cuál es el valor de Ea inversa? (c) ¿cuál es el valor del ∆H de la reacción directa?
1 point
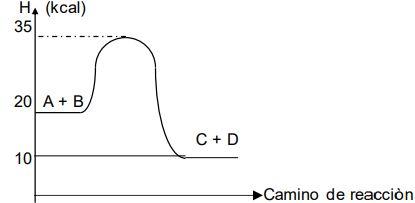
A) (a)15 kcal, (b) 25 kcal, (c) -10 kcal
B) (a) 35 kcal, (b) 25 kcal, (c) -10 kcal
C) (a)15 kcal, (b) 15 kcal, (c) 10 kcal
D) (a) 35 kcal, (b) 35 kcal, (c) -10 kcal
E) (a)10 kcal, (b) 25 kcal, (c) -15 kcal
3. La constante de velocidad para una reacción de primer orden cuya vida media es de 1602 segundos, es:
1 point
A) 4,32.10⁻⁴ s⁻¹
B) 0,026 min⁻¹
C) 7,21.10⁻⁶ min⁻¹
D) 0,026 s⁻¹
E) màs de una
4. La afirmación correcta con respecto a un catalizador, es:
1 point
A) disminuye la entalpía de reacción
B) disminuye la energía de los reactivos
C) aumenta la energía de activación
D) no altera las leyes de la rapidez
E) altera los mecanismo de reacción
5.

A) I, II y III
B) Solo I y III
C) Solo III
D) Solo I
E) I y II
6.
A) 24,5
B) 6,9
C) 26,9
D) 0,04
E) 0,14
7. Teniendo en cuenta los siguientes datos experimentales; la expresión de la velocidad de la reacción es:
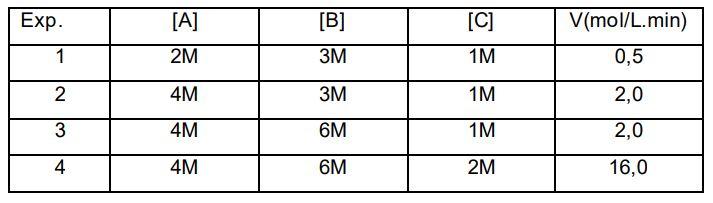
A) V=k[A]³ [C]²
B) V=k[A] [B]² [C]
C) V=k[A]² [C]²
D) V=k[A]² [B]³ [C]
E) V=k[A]² [C]³
8. En un recipiente de 200 mL de capacidad se colocan a baja temperatura 0,40 g de tetróxido de dinitrógeno, se cierra y se calienta a 45°C; el N₂O₄ se vaporiza y se disocia en un 41,6% en NO₂; la constante de equilibrio, es: (PA: N=14, O=16)
A) 0,0514
B) 0,0128
C) 0,0086
D) 0,0257
E) 0,1028
9. Para la reacción exotérmica; 2 SO₂ (g) + O₂ (g) ↔ 2 SO₃ (g) ; de los siguientes factores, el que NO afecta el equilibrio, es:
A) cambios en la concentración de O₂ (g)
B) aumento de la presión
C) aumento de volumen
D) presencia de un catalizador
E) aumento de la temperatura
10. Se prepara una solución por agitación de 1 gramo de fluoruro de calcio en 1,00 L de agua a 25°C. Un análisis indica que se disolvió 0,0163 g de fluoruro de calcio. El valor de Kps de dicha sal, es: (Pesos atòmicos: Ca=40 , F=19)
A) 2,46.10⁻¹⁰
B) 3,65.10⁻¹¹
C) 1,73.10⁻⁵
D) 8,42.10⁻⁶
E) 9,12.10⁻¹²