Sales neutras de acido oxacidos
- 이온화합물
- 산과 염기의 완전한 중화neutralizacion total를 통해 얻게 된당
- 음이온 생성물을 생성함genera el anion de la sal (hidroxido: 양이온 생성물을 생성genera el cation de la sal)

| 명명법 | |
| IUPAC | oxianion + metal (nox) |
| Tradición | oxianion + metal -oso/ -ico |
ex)
| Ca(ClO3)2 | clorato de calcio |
| NaClO | hipoclorito de sodio |
| Fe(AsO2)3 | metaarsenito de hierro (III) |
수화물, 수화생성물 hidratos o sales hidratadas
AB(sal) x nH2O
명명법: Sal 이름 + prefijo + 수화물hidratados
- cuaternarias 사차화합물!
| MgSO4 x 7H2O | sulfato de magnesio heptahidratado |
| CuSO4 x 5H2O | sulfato cuprico pentahidratado |
| BaCl2 x 2H2O | cloruro de bario dihidratado |
시안화물Cianuros
- 시안화산ac. cianhidrico(HCN) 에서 온 화합물
- 이온화합물
- 시안화물은 인간을 죽음에 이르게할만큼 치명적인 독임. 그... 복어에 들어있는거랑 사과에 있는 독이 이거고 (사과 씨앗) 이게 미토콘드리아의 세포호흡을 막아서 ATP 생산을 멈추게 한다.
갑분생물학....
시안화산ac. cianhidrico(HCN) ⇀ 시안화이온 CN-
화학식 표기:

명명법: cianuro + 메탈이름
| cianuro de potasio | KCN |
| cianuro de sodio | NaCN |
사차 화합물combinaciones cuaternarias
산성 생성물sales acidas
염기에 의한 산의 부분적 중화neutralizacion parcial에서 온다
명명법nomenclatura:
| IUPAC | 음이온 이름 + prefijo (남은 H 개수를 의미) + 산acido + 메탈의 이름 (nox) |
| Tradición | 음이온 이름 + prefijo (남은 H 개수를 의미) + 산acido + 메탈 (-oso, -ico) |
| fosfato biacido de sodio | NaH2PO4 |
| piroarseniato triacido de calcio | Ca(H3As2O7)2 |
ex) piroantimonito biacido férrico
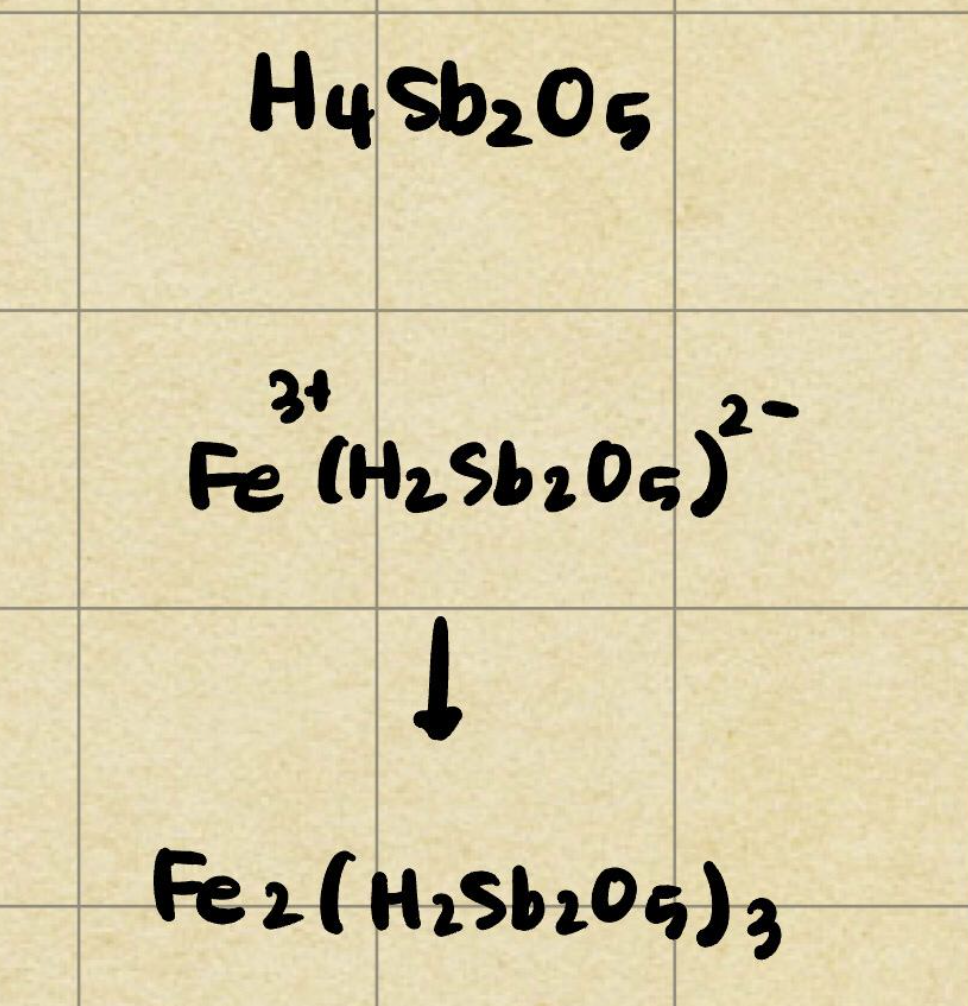
산성 생성물은 크게 두가지로 나뉜다
| 산성 생성물sales acidas: 염기에 의한 산의 부분적 중화neutralizacion parcial에서 온다 |
||
| a) 이양성자산acido diprotico에서 온 산성생성물 이양성자산: 말그대로 수소 2개가진 산들 ex) H2CO3, H2SO3, H2SO4, H2SeO3, H2SeO4, H2TeO3 |
tradicion | oxiaion (mono)acido + 금속에서온 접미사raiz de metal -iso/-oso |
| 더 자주 쓰이는 것 | bi + 음이온 이름 + 메탈이름 | |
| ex) | NaHCO3 탄산수소나트륨 carbonato monoacido de sodio (bicarbonato de sodio) ⇨ H2CO3 에서 옴! |
|
| KHSO4 sulfato monoacido de potasio (bisulfato de potasio) ⇨ H2SO4 에서 옴! |
||
| b) 다른 acido oxacido에서 온 산성생성물 생성물sal - monoacido: 1H 수소 하나가 남음 - biacidas: 2H 수소 두개가 남음 - triacidas: 3H 수소 세개가 남음 |
예시) | CoH2As2O5 piroarsenito biacido cobaltoso Fe(H2PO3)2 fosfito monoacido ferroso *여기서 H 하나는 산이고 다른 하나는 중성neutro임! |
염기 생성물sales básicos
- 산에 의한 염기의 부분적 중화neutralizacion parcial에서 온다
- 이온화합물!
- 명명법: 음이온 이름 + (mono, bi, tri) 염기와 메탈에서 온 접미어 basico raiz del nombre del metal + oso/ico
| 생성물sal |
monobasica: OH 하나가 남음 |
| bibasica: OH 두개가 남음 | |
| tribasica: OH 세개가 남음 |
예시)
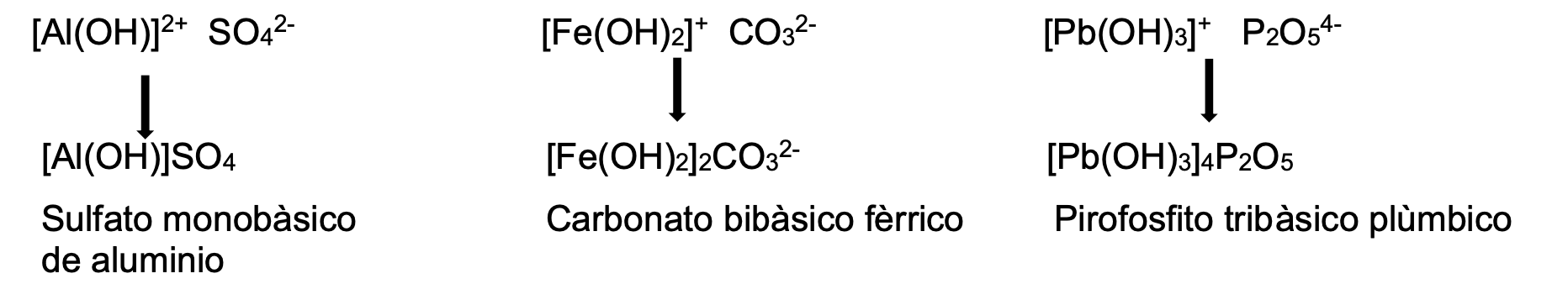
암모늄 염sales de Amonio
- 암모늄 이온 (NH4)+에서 온것들
- 명명법: 음이온 이름 + de amonio
| sulfato de amonio | (NH4)2SO4 |
| fosfato de amonio | (NH4)3PO4 |
✴️✴️✴️예외!!! 생긴건 암모늄 염인에 4차 화합물이 아닌 3차 화합물compuesto ternaria인것들
| nitrato de amonio | (NH4)NO3 |
| nitrito de amonio | (NH4)NO2 |
| cloruro de amonio | (NH4)Cl |
화학양론estequiometria de la composicion
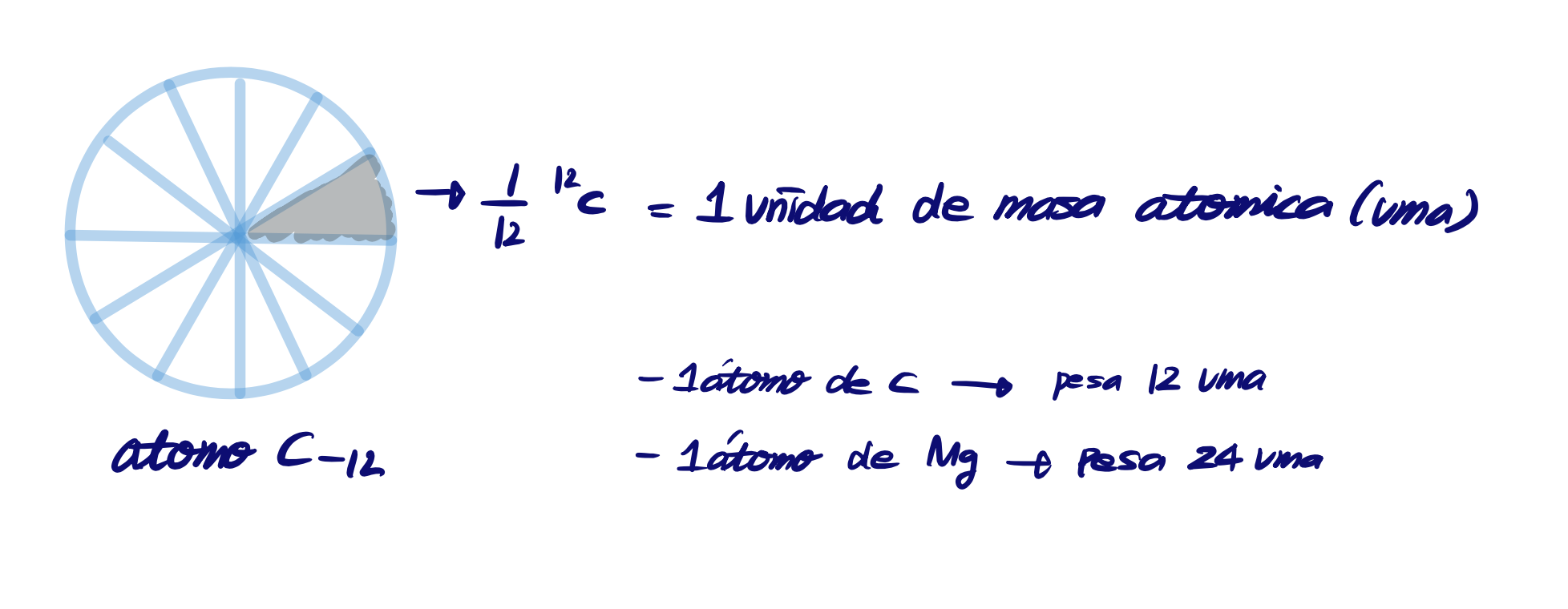
원자질량, 원자무게masa atómica, peso atómica (단위: uma)
원자하나의 질량
평균원자질량masa atómica promedio
서로다른 동위원소의 질량 평균이당
1 H ⇀ 1.0 (98%)
2 H ⇀ 2.0 (1.8%)
3 H ⇀ 3.0 (0.2%)
공식: 평균원자질량 구하기

예시
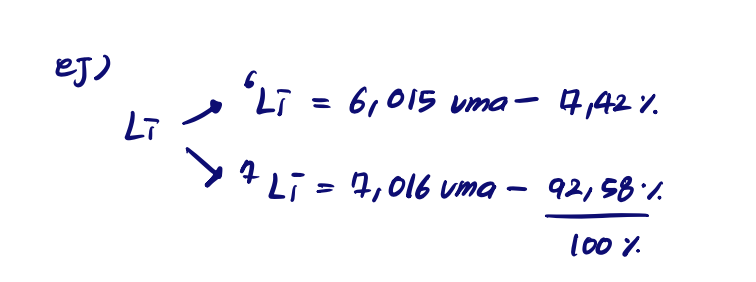

공식 질량 masa formular (단위: uma)
- 이온결합, 공유결합 화합물에 쓰인다
- 분자에도 쓰일 수 있음
1) sulfato de aluminio Al2(SO4)3
Al: 2x 27 = 54 uma
S: 3x 32 = 96 uma
O: 12x 16 = 192 uma
총합: 342 uma
2) fosfato del calcio Ca3(PO4)2
Al: 3x 40.08 = 120.24 uma
P: 3x 30.97 = 92.91 uma
O: 8x 16 = 128 uma
총합: 341.15 uma
분자질량 masa molecular (단위: uma)
- 분자에 쓰인다
- 공유 화합물에만 쓸수 있는 표현!
ex)포도당 C6H12O6
몰mol
모든 원자, 분자, 이온이 가지는 물질의 양
탄소원자는 12g을 가짐
1mol ⇀ 6,02 x 10 23 particulas 입자수
* 6,02 x 10 23: 아보가드로 수número de avogadro

H2O 물분자 하나
- 18uma 무게가 나감
- 원자 3개로 이루어져있다 (수소원자 2, 산소원자 1)
H2O 물의 몰 하나
- 6.02 x 10 23 물 분자를 가진다
- 3개의 몰원자를 가진다 ( 수소원자 분자 2개 / 산소원자 분자 1개 )
수소원자의 아보가드로 수: 2 x 6.02 x 10 23 개
산소원자의 아보가드로 수: 1 x 6.02 x 10 23 개
1. 1000개 물분자에는 몇개의 O 원자가 있는가?
물 분자 하나 - 1개의 산소원자
1000개의 물분자 - x
답: 1000개의 산소원자를 가짐
2. 25몰의 물에있는 몰 원자 수는?
물 1몰 - 3개의 원자몰 (수소+산소..)
물 25몰 - 75개의 원자몰을 가진다!
3. 물 150몰에는 몇개의 수소원자가 있는가?
1mol de H2O - 2x 6.02 x 2 x 6.02 x 10 23 개
150 moles - x
x = 1.806 x 10 26 개의 수소원자!
몰 질량masa molar (단위: 그램g)
몰 하나의 질량 or 6.02 x 10^23 입자 (원자, 분자, 이온)
원자 질량, 분자질량, 공식질량을 g그램으로 바꾼것! 다시말하면 값에는 변화가 없다는것. 걍 단위만 그램으로 바꿔준거!
탄소 1몰 - 12g
리튬 원자 1몰- 6.941g de Li
ex) Na ⇀ masa atomica: 23 uma
⇀ 1 mol de atomos de Na: 23 gramos
H2O ⇀ masa molecular: 18 uma
⇀ 1 mol de atomos de Na:18 gramos
NaCl ⇀ masa ion - formula: 58.5 uma
⇀ 1 mol de iones - formula:58.5 gramos
그램과 uma의 관계성

나트륨 원자 하나 1 atomo de Na: 23 uma
나트륨 원자 1몰 1 mol de atomos de Na: 23 g
나트륨 원자 1몰1 mol de atomos de Na: 6.02 x 10 23 atomos de Na
화학식과 조성 백분율 ★
화학식과 조성 백분율 --------------------------------------------------- ▶ 조성 백분율 (Percent Composition) > 물질을 구성하는 각 원자의 질량 백분율 (단위: %) ---> 조성 백분율 = 질량 백분율 ( 참고..
ywpop.tistory.com
화학식과 조성 백분율composicion porcentual
100g 질량의 화합물을 백분율 (%) 로 나타낸 것


예시) 에탄올 C2H5OH (PM 화학식량: 46.07 uma)

예시문제)
헤모글로빈에는 0.335% 의 철이있음
헤모글로빈 분자하나는 1개의 철원자를 가질때, 헤모글로빈의masa molar은?

실험식formula empírica ( o minima)

분자식formula molecular
'UNA MED 재수 2022 > 화학 (Quimica)' 카테고리의 다른 글
| [Quimica] test 오답풀이 (0) | 2022.05.07 |
|---|---|
| [quimica] guia 6 - nomenclatura (무기화학 명명법) (0) | 2022.05.06 |
| [quimica] (guia 6, semanal 6) hibridacion 혼성오비탈 (0) | 2022.04.30 |
| [quimica] guia 5 내용정리 (0) | 2022.04.22 |
| [quimica] guia 4 (semanal 4) (0) | 2022.04.16 |




댓글